Bieżący numer
Artykuły zaakceptowane
O czasopiśmie
Rada Naukowa
Kolegium Redakcyjne
Polityka prawno-archiwizacyjna
Kodeks etyki publikacyjnej
Wydawca
Informacja o przetwarzaniu danych osobowych w ramach plików cookies oraz subskrypcji newslettera
Archiwum
Dla autorów
Dla recenzentów
Kontakt
Recenzenci
Recenzenci rocznika 2025
Recenzenci rocznika 2024
Recenzenci rocznika 2023
Recenzenci rocznika 2022
Recenzenci rocznika 2021
Recenzenci rocznika 2020
Recenzenci rocznika 2019
Recenzenci rocznika 2018
Recenzenci rocznika 2017
Recenzenci rocznika 2016
Recenzenci rocznika 2015
Recenzenci rocznika 2014
Recenzenci rocznika 2013
Recenzenci rocznika 2012
Polecamy
Śląski Uniwersytet Medyczny w Katowicach
Sklep Wydawnictw SUM
Biblioteka Główna SUM
Polityka prywatności
Deklaracja dostępności
Recenzenci
Recenzenci rocznika 2025
Recenzenci rocznika 2024
Recenzenci rocznika 2023
Recenzenci rocznika 2022
Recenzenci rocznika 2021
Recenzenci rocznika 2020
Recenzenci rocznika 2019
Recenzenci rocznika 2018
Recenzenci rocznika 2017
Recenzenci rocznika 2016
Recenzenci rocznika 2015
Recenzenci rocznika 2014
Recenzenci rocznika 2013
Recenzenci rocznika 2012
Ocena właściwości fotoprotekcyjnych opakowań farmaceutycznych zawierających cefuroksym za pomocą analizy hemisferycznej reflektancji całkowitej
1
Department of Basic Biomedical Sciences, Faculty of Pharmaceutical Sciences in Sosnowiec, Medical University of Silesia, Katowice, Poland
2
Doctoral School, Faculty of Pharmaceutical Sciences in Sosnowiec, Medical University of Silesia, Katowice, Poland
Autor do korespondencji
Michał Meisner
Katedra i Zakład Podstawowych Nauk Biomedycznych, Wydział Nauk Farmaceutycznych w Sosnowcu, Śląski Uniwersytet Medyczny w Katowicach, ul. Jedności 10, 41-200 Sosnowiec
Katedra i Zakład Podstawowych Nauk Biomedycznych, Wydział Nauk Farmaceutycznych w Sosnowcu, Śląski Uniwersytet Medyczny w Katowicach, ul. Jedności 10, 41-200 Sosnowiec
Ann. Acad. Med. Siles. 2024;78:226-233
SŁOWA KLUCZOWE
hemisferyczna reflektancja kierunkowaopakowania bezpośrednieopakowania zewnętrzneantybiotykicefuroksym
DZIEDZINY
STRESZCZENIE
Wstęp:
Niewłaściwe zabezpieczenie substancji czynnej może doprowadzić do utraty jej pierwotnych właściwości. Do oceny własności fotoprotekcyjnych opakowań leków można zastosować wiele metod, w tym hemisferyczną reflektancję kierunkową. Celem badania była ocena wartości reflektancji dla opakowania zewnętrznego (pudełko kartonowe) i opakowania bezpośredniego (blister) zawierającego cefuroksym.
Materiał i metody:
Za pomocą reflektometru 410-Solar zbadano opakowania dwóch preparatów (Ceroxim i Zinnat), zarówno przeterminowanych, jak i nieprzeterminowanych. Analizie poddano trzy rodzaje obszarów pomiarowych: „biały” (biały karton zewnętrzny), „kolorowy” (obszary kolorystyczne kartonu zewnętrznego) oraz „blister” (opakowanie bezpośrednie wykonane z aluminium i PCV).
Wyniki:
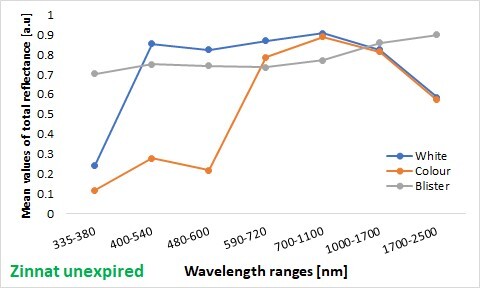
Największą wartość reflektancji stwierdzono w zakresie 700–1100 nm zarówno dla preparatów przeterminowanych, jak i nieprzeterminowanych. W zakresie 335–380 nm ilość odbitego promieniowania dla nieprzeterminowanych opakowań Ceroxim vs Zinnat wynosiła odpowiednio: 30% vs 12% dla obszarów kolorowych, 39% vs 24% dla obszarów białych i 74% vs 70% dla blistrów. W przypadku preparatu Ceroxim, reflektancja nieprzeterminowanych obszarów kolorowych była znacząco wyższa niż przeterminowanych (p < 0,001) we wszystkich zakresach spektralnych, z wyjątkiem 1700–2500 nm. Natomiast reflektancja przeterminowanych obszarów białych preparatu Ceroxim była wyższa niż nieprzeterminowanych (p < 0,001) dla 480–600 nm, 590–720 nm, 700–1100 nm i 1700–2500 nm. Blistry nieprzeterminowane preparatu Zinnat wykazywały mocniejsze właściwości fotoprotekcyjne niż przeterminowane w zakresie 335–380 nm. Nie stwierdzono różnic pomiędzy przeterminowanymi i nieprzeterminowanymi blistrami preparatu Ceroxim.
Wnioski:
Wartość reflektancji wskazuje, że blistry i opakowania z białego kartonu w większym stopniu chronią cefuroksym przed promieniowaniem niż opakowania kolorowe.
Niewłaściwe zabezpieczenie substancji czynnej może doprowadzić do utraty jej pierwotnych właściwości. Do oceny własności fotoprotekcyjnych opakowań leków można zastosować wiele metod, w tym hemisferyczną reflektancję kierunkową. Celem badania była ocena wartości reflektancji dla opakowania zewnętrznego (pudełko kartonowe) i opakowania bezpośredniego (blister) zawierającego cefuroksym.
Materiał i metody:
Za pomocą reflektometru 410-Solar zbadano opakowania dwóch preparatów (Ceroxim i Zinnat), zarówno przeterminowanych, jak i nieprzeterminowanych. Analizie poddano trzy rodzaje obszarów pomiarowych: „biały” (biały karton zewnętrzny), „kolorowy” (obszary kolorystyczne kartonu zewnętrznego) oraz „blister” (opakowanie bezpośrednie wykonane z aluminium i PCV).
Wyniki:
Największą wartość reflektancji stwierdzono w zakresie 700–1100 nm zarówno dla preparatów przeterminowanych, jak i nieprzeterminowanych. W zakresie 335–380 nm ilość odbitego promieniowania dla nieprzeterminowanych opakowań Ceroxim vs Zinnat wynosiła odpowiednio: 30% vs 12% dla obszarów kolorowych, 39% vs 24% dla obszarów białych i 74% vs 70% dla blistrów. W przypadku preparatu Ceroxim, reflektancja nieprzeterminowanych obszarów kolorowych była znacząco wyższa niż przeterminowanych (p < 0,001) we wszystkich zakresach spektralnych, z wyjątkiem 1700–2500 nm. Natomiast reflektancja przeterminowanych obszarów białych preparatu Ceroxim była wyższa niż nieprzeterminowanych (p < 0,001) dla 480–600 nm, 590–720 nm, 700–1100 nm i 1700–2500 nm. Blistry nieprzeterminowane preparatu Zinnat wykazywały mocniejsze właściwości fotoprotekcyjne niż przeterminowane w zakresie 335–380 nm. Nie stwierdzono różnic pomiędzy przeterminowanymi i nieprzeterminowanymi blistrami preparatu Ceroxim.
Wnioski:
Wartość reflektancji wskazuje, że blistry i opakowania z białego kartonu w większym stopniu chronią cefuroksym przed promieniowaniem niż opakowania kolorowe.
REFERENCJE (13)
1.
Waterman K.C., MacDonald B.C. Package selection for moisture protection for solid, oral drug products. J. Pharm. Sci. 2010; 99(11): 4437–4452, doi: 10.1002/jps.22161.
2.
Poitou P. The role of the packaging in terms of safety and good use of medicines. [Article in French]. Ann. Pharm. Fr. 2003; 61(5): 300–303.
3.
McPherson T., Kolling W.M. Stability and compatibility study guidelines for AJHP. Am. J. Health Syst. Pharm. 2023; 80(18): 1271–1274, doi: 10.1093/ajhp/zxad132.
4.
Berendsen B.J.A., Elbers I.J.W., Stolker A.A.M. Determination of the stability of antibiotics in matrix and reference solutions using a straightforward procedure applying mass spectrometric detection. Food Addit. Contam. Part A Chem. Anal. Control Expo. Risk Assess. 2011; 28(12): 1657–1666, doi: 10.1080/19440049.2011.604045.
5.
Bhutani H., Mariappan T.T., Singh S. The physical and chemical stability of anti-tuberculosis fixed-dose combination products under accelerated climatic conditions. Int. J. Tuberc. Lung Dis. 2004; 8(9): 1073–1080.
6.
Lin X., Kück U. Cephalosporins as key lead generation beta-lactam antibiotics. Appl. Microbiol. Biotechnol. 2022; 106(24): 8007–8020, doi: 10.1007/s00253-022-12272-8.
7.
Błoński B., Wilczyński S., Hartman-Petrycka M., Michalecki Ł. The use of hemispherical directional reflectance to evaluate the interaction of food products with radiation in the solar spectrum. Foods 2022; 11(13): 1974, doi: 10.3390/foods11131974.
8.
Kundu P., Bandyopadhyay S., Trémeau A. Analysis of spectral differences between printers to detect the counterfeit medicine packaging. J. Algebr. Stat. 2022; 13(2): 798–806.
9.
Çapkın İ.Y., Gökelma M. A review on characterization and recyclability of pharmaceutical blisters. Cleaner Waste Systems 2023; 4: 100082, doi: 10.1016/j.clwas.2023.100082.
10.
Matyukhin P.V. The choice of iron-containing filling for composite radioprotective material. IOP Conf. Ser.: Mater. Sci. Eng. 2018; 327: 032036, doi: 10.1088/1757-899X/327/3/032036.
11.
Li X., Yang J., Qiao Y., Duan Y., Xin Y., Nian Y. et al. Effects of radiation on drug metabolism: A review. Curr. Drug Metab. 2019; 20(5): 350–360, doi: 10.2174/1389200220666190405171303.
12.
McGill M.R., Findley D.L., Mazur A., Yee E.U., Allard F.D., Powers A. et al. Radiation effects on methamphetamine pharmacokinetics and pharmacodynamics in rats. Eur. J. Drug Metab. Pharmacokinet. 2022; 47(3): 319–330, doi: 10.1007/s13318-022-00755-y.
13.
Glass B.D., Novák C., Brown M.E. The thermal and photostability of solid pharmaceuticals. J. Therm. Anal. Calorim. 2004; 77: 1013–1036, doi: 10.1023/B:JTAN.0000041677.48299.25.
CYTOWANIA (1):
1.
The Impact of UV Radiation on the Hemispherical Reflectance Values and Homogeneity of Tablets Containing Clindamycin and Phenoxymethylpenicillin
Michał Meisner, Beata Sarecka-Hujar
Applied Sciences
Michał Meisner, Beata Sarecka-Hujar
Applied Sciences
Udostępnij
Śląski Uniwersytet Medyczny w Katowicach, jako Operator Serwisu annales.sum.edu.pl, przetwarza dane osobowe zbierane podczas odwiedzania Serwisu. Realizacja funkcji pozyskiwania informacji o Użytkownikach i ich zachowaniu odbywa się poprzez dobrowolnie wprowadzone w formularzach informacje, zapisywanie w urządzeniach końcowych plików cookies (tzw. ciasteczka), a także poprzez gromadzenie logów serwera www, będącego w posiadaniu Operatora Serwisu. Dane, w tym pliki cookies, wykorzystywane są w celu realizacji usług zgodnie z Polityką prywatności.
Możesz wyrazić zgodę na przetwarzanie danych w tych celach, odmówić zgody lub uzyskać dostęp do bardziej szczegółowych informacji.
Możesz wyrazić zgodę na przetwarzanie danych w tych celach, odmówić zgody lub uzyskać dostęp do bardziej szczegółowych informacji.