Bieżący numer
Artykuły zaakceptowane
O czasopiśmie
Rada Naukowa
Kolegium Redakcyjne
Polityka prawno-archiwizacyjna
Kodeks etyki publikacyjnej
Wydawca
Informacja o przetwarzaniu danych osobowych w ramach plików cookies oraz subskrypcji newslettera
Archiwum
Dla autorów
Dla recenzentów
Kontakt
Recenzenci
Recenzenci rocznika 2025
Recenzenci rocznika 2024
Recenzenci rocznika 2023
Recenzenci rocznika 2022
Recenzenci rocznika 2021
Recenzenci rocznika 2020
Recenzenci rocznika 2019
Recenzenci rocznika 2018
Recenzenci rocznika 2017
Recenzenci rocznika 2016
Recenzenci rocznika 2015
Recenzenci rocznika 2014
Recenzenci rocznika 2013
Recenzenci rocznika 2012
Polecamy
Śląski Uniwersytet Medyczny w Katowicach
Sklep Wydawnictw SUM
Biblioteka Główna SUM
Polityka prywatności
Deklaracja dostępności
Recenzenci
Recenzenci rocznika 2025
Recenzenci rocznika 2024
Recenzenci rocznika 2023
Recenzenci rocznika 2022
Recenzenci rocznika 2021
Recenzenci rocznika 2020
Recenzenci rocznika 2019
Recenzenci rocznika 2018
Recenzenci rocznika 2017
Recenzenci rocznika 2016
Recenzenci rocznika 2015
Recenzenci rocznika 2014
Recenzenci rocznika 2013
Recenzenci rocznika 2012
Analiza zawartości maślanu sodu w różnych suplementach diety dostępnych na polskim rynku
1
Department of Internal Medicine and Clinical Pharmacology, Faculty of Medical Sciences in Katowice, Medical University of Silesia, Katowice, Poland
Autor do korespondencji
Maciej Borówka
Klinika Chorób Wewnętrznych i Farmakologii Klinicznej, ul. Medyków 14, 40-752 Katowice, Uniwersyteckie Centrum Kliniczne im. prof. K. Gibińskiego ŚUM
Klinika Chorób Wewnętrznych i Farmakologii Klinicznej, ul. Medyków 14, 40-752 Katowice, Uniwersyteckie Centrum Kliniczne im. prof. K. Gibińskiego ŚUM
SŁOWA KLUCZOWE
DZIEDZINY
STRESZCZENIE
Wstęp:
Maślan sodu jest związkiem chemicznym, któremu przypisuje się liczne korzystne właściwości biologiczne, w tym zdolność łagodzenia objawów chorób przewodu pokarmowego. W konsekwencji stał się on częstym składnikiem terapii wspomagających. Wszystkie doustne preparaty zawierające maślan sodu dostępne na polskim rynku są jednak zarejestrowane jako suplementy diety, a żaden z nich nie posiada statusu produktu leczniczego, co może budzić wątpliwości dotyczące ich jakości.
Materiał i metody:
Maślan sodu z ośmiu różnych suplementów diety dostępnych na polskim rynku w kwietniu 2024 r. został wyekstrahowany z użyciem eteru dietylowego. Następnie eter odparowano, a pozostałość rozpuszczono w metanolu w celu przeprowadzenia wysokosprawnej chromatografii cieczowej (high-performance liquid chromatography – HPLC). Otrzymane roztwory przepuszczono przez kolumnę chromatograficzną, aby oznaczyć dokładną zawartość maślanu sodu w każdej próbce. Uzyskane piki porównano ze wzorcami i finalnie obliczono zawartość maślanu sodu w poszczególnych próbkach.
Wyniki:
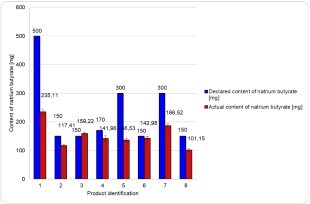
Zawartość maślanu sodu wykryto we wszystkich analizowanych próbkach. Jednak stosunek ilości oznaczonej do deklarowanej przez producenta wahał się od 45.51% do 106.15%.
Wnioski:
W większości przypadków analizowane suplementy diety zawierały maślan sodu w ilościach zbliżonych do deklarowanych przez producentów, jednak zgodność z deklaracją producenta różniła się pomiędzy konkretnymi produktami, co podkreśla konieczność dalszych badań w tym zakresie.
Maślan sodu jest związkiem chemicznym, któremu przypisuje się liczne korzystne właściwości biologiczne, w tym zdolność łagodzenia objawów chorób przewodu pokarmowego. W konsekwencji stał się on częstym składnikiem terapii wspomagających. Wszystkie doustne preparaty zawierające maślan sodu dostępne na polskim rynku są jednak zarejestrowane jako suplementy diety, a żaden z nich nie posiada statusu produktu leczniczego, co może budzić wątpliwości dotyczące ich jakości.
Materiał i metody:
Maślan sodu z ośmiu różnych suplementów diety dostępnych na polskim rynku w kwietniu 2024 r. został wyekstrahowany z użyciem eteru dietylowego. Następnie eter odparowano, a pozostałość rozpuszczono w metanolu w celu przeprowadzenia wysokosprawnej chromatografii cieczowej (high-performance liquid chromatography – HPLC). Otrzymane roztwory przepuszczono przez kolumnę chromatograficzną, aby oznaczyć dokładną zawartość maślanu sodu w każdej próbce. Uzyskane piki porównano ze wzorcami i finalnie obliczono zawartość maślanu sodu w poszczególnych próbkach.
Wyniki:
Zawartość maślanu sodu wykryto we wszystkich analizowanych próbkach. Jednak stosunek ilości oznaczonej do deklarowanej przez producenta wahał się od 45.51% do 106.15%.
Wnioski:
W większości przypadków analizowane suplementy diety zawierały maślan sodu w ilościach zbliżonych do deklarowanych przez producentów, jednak zgodność z deklaracją producenta różniła się pomiędzy konkretnymi produktami, co podkreśla konieczność dalszych badań w tym zakresie.
FINANSOWANIE
Niniejsze badania nie były finansowane ze środków zewnętrznych. Autorzy nie mają do ujawnienia żadnych interesów finansowych czy niefinansowych.
KONFLIKT INTERESÓW
Autorzy deklarują brak konfliktu interesów.
REFERENCJE (17)
1.
Morrison DJ, Preston T. Formation of short chain fatty acids by the gut microbiota and their impact on human metabolism. Gut Microbes. 2016;7(3):189–200. doi: 10.1080/19490976.2015.1134082.
2.
Wong JMW, de Souza R, Kendall CWC, Emam A, Jenkins DJA. Colonic health: fermentation and short chain fatty acids. J Clin Gastroenterol. 2006;40(3):235–243. doi: 10.1097/00004836-200603000-00015.
3.
Lewandowski K, Kaniewska M, Karłowicz K, Rosołowski M, Rydzewska G. The effectiveness of microencapsulated sodium butyrate at reducing symptoms in patients with irritable bowel syndrome. Prz Gastroenterol. 2022;17(1):28–34. doi: 10.5114/pg.2021.112681.
4.
Scarpellini E, Lauritano EC, Lupascu A, Petruzzellis C, Novi ML, Roccarina D, et al. Efficacy of butyrate in the treatment of diarrhoea-predominant irritable bowel syndrome. Dig Liver Dis Suppl. 2007;1(1):19–22. doi: 10.1016/S1594-5804(08)60006-6.
5.
Facchin S, Vitulo N, Calgaro M, Buda A, Romualdi C, Pohl D, et al. Microbiota changes induced by microencapsulated sodium butyrate in patients with inflammatory bowel disease. Neurogastroenterol Motil. 2020;32(10):e13914. doi: 10.1111/nmo.13914.
6.
Recharla N, Geesala R, Shi XZ. Gut microbial metabolite butyrate and its therapeutic role in inflammatory bowel disease: A literature review. Nutrients. 2023;15(10):2275. doi: 10.3390/nu15102275.
7.
Mayorga-Ramos A, Barba-Ostria C, Simancas-Racines D, Guamán LP. Protective role of butyrate in obesity and diabetes: New insights. Front Nutr. 2022;9:1067647. doi: 10.3389/fnut.2022.1067647.
8.
Peng K, Dong W, Luo T, Tang H, Zhu W, Huang Y, et al. Butyrate and obesity: Current research status and future prospect. Front Endocrinol (Lausanne). 2023;14:1098881. doi: 10.3389/fendo.2023.1098881.
9.
Obwieszczenie Ministra Zdrowia z dnia 23 grudnia 2022 r. w sprawie ogłoszenia jednolitego tekstu rozporządzenia Ministra Zdrowia w sprawie składu oraz oznakowania suplementów diety. Dz.U. 2023 poz. 79.
10.
Ustawa z dnia 6 września 2001 r. Prawo farmaceutyczne. Dz.U. 2001 nr 126 poz. 1381.
11.
Dwyer JT, Coates PM, Smith MJ. Dietary supplements: regulatory challenges and research resources. Nutrients. 2018;10(1):41. doi: 10.3390/nu10010041.
12.
Ronis MJJ, Pedersen KB, Watt J. Adverse effects of nutraceuticals and dietary supplements. Annu Rev Pharmacol Toxicol. 2018;58:583–601. doi: 10.1146/annurev-pharmtox-010617-052844.
13.
De Baere S, Eeckhaut V, Steppe M, De Maesschalck C, De Backer P, Van Immerseel F, et al. Development of a HPLC-UV method for the quantitative determination of four short-chain fatty acids and lactic acid produced by intestinal bacteria during in vitro fermentation. J Pharm Biomed Anal. 2013;80:107–115. doi: 10.1016/j.jpba.2013.02.032.
14.
Eberhart BL 2nd, Wilson AS, O’Keefe SJD, Ramaboli MC, Nesengani LT. A simplified method for the quantitation of short-chain fatty acids in human stool. Anal Biochem. 2021;612:114016. doi: 10.1016/j.ab.2020.114016.
15.
Maćkiewicz E, Klimaszewska M, Albińska J, Szynkowska-Jóźwik MI. Evaluation of the elemental composition of dietary supplements containing iron available on the Polish market using ICP-OES, FAAS and CVAAS techniques. Molecules. 2025;30(23):4511. doi: 10.3390/molecules30234511.
16.
Wołonkiewicz K, Podolak I, Paśko P, Galanty A. Analysis of caffeine content in weight-loss dietary supplements. Farm Pol. 2019;75(2):53–56. doi: 10.32383/farmpol/116302.
17.
Puścion-Jakubik A, Bartosiewicz N, Socha K. Is the Magnesium Content in Food Supplements Consistent with the Manufacturers’ Declarations? Nutrients. 2021;13(10):3416. doi: 10.3390/nu13103416.
Udostępnij
Śląski Uniwersytet Medyczny w Katowicach, jako Operator Serwisu annales.sum.edu.pl, przetwarza dane osobowe zbierane podczas odwiedzania Serwisu. Realizacja funkcji pozyskiwania informacji o Użytkownikach i ich zachowaniu odbywa się poprzez dobrowolnie wprowadzone w formularzach informacje, zapisywanie w urządzeniach końcowych plików cookies (tzw. ciasteczka), a także poprzez gromadzenie logów serwera www, będącego w posiadaniu Operatora Serwisu. Dane, w tym pliki cookies, wykorzystywane są w celu realizacji usług zgodnie z Polityką prywatności.
Możesz wyrazić zgodę na przetwarzanie danych w tych celach, odmówić zgody lub uzyskać dostęp do bardziej szczegółowych informacji.
Możesz wyrazić zgodę na przetwarzanie danych w tych celach, odmówić zgody lub uzyskać dostęp do bardziej szczegółowych informacji.